对包含二氧化锰浸渍凝胶聚合物电解质的阀控铅酸电池电化学行为的理解状态
对包含二氧化锰浸渍凝胶聚合物电解质的阀控铅酸电池电化学行为的理解状态
在过去的几十年里,新的研究计划侧重于创建增强型铅酸电池,通过使用目前正在开发的创新材料来提高功率、耐用性和可靠性。1最流行的可充电电池仍然是铅酸电池,它用于许多不同的领域,包括电信、太阳能交通灯、不间断电源、固定和牵引应用以及汽车。尽管价格便宜,但与其他创新储能方法相比,铅酸电池的能量密度较低。快速充电或许能够解决铅酸电池在特定应用中的缺点,例如多用途车辆和叉车。在短暂停顿期间可快速充电的多用途汽车的性能几乎与具有更先进电池的汽车一样。2氧循环的管理、板栅合金和隔膜的设计以及充电方法的优化都需要在阀控式铅酸(VRLA)电池从其淹没式母电池的发展过程中付出巨大的技术努力。几年。3由于 VRLA 电池具有维护成本低、安装简单(即使在通勤设备的机架中)、无气体释放、生产清洁产品以及价格实惠等固有品质,因此成为储能的首选。4
在 VRLA 电池的构造中,使硫酸溶液胶凝并随后固定电解质是关键阶段。5凝胶聚合物电解质通常是溶胀的聚合物网络,因此从扩散传输的角度来看,它们既具有固体的内聚特性,又具有液体的特性。6近年来,一些聚合物如聚甲基丙烯酸甲酯、7聚丙烯酰胺、8海藻酸钙、9聚丙烯腈 (PAN) 10和聚乙烯醇11已用于制备凝胶电解质。当聚醋酸乙烯酯经过醇解、水解或氨解时,会产生一种称为聚乙烯醇(PVA)的长链水溶性聚合物。基于 PVA 的水凝胶是一种胶体分散体,具有溶胀和交联作用,可形成三维网络结构。12由于 PVA 基凝胶电解质低毒、易获得、经济实惠且环境友好,因此受到了广泛的研究关注。13聚合物电解质的产生是由主体基质 PVA 中的 –OH 基团引起的,该基团与主链碳链的甲烷碳相连。14储能装置的性能受到其典型的保水能力弱、大幅变形下快速疲劳以及导电性差等问题的严重制约。15 PVA 的缺点可以通过添加金属氧化物、导电聚合物、纳米材料等增塑剂来克服。Wang等人。报道称PVA可用于制备多功能凝胶电解质复合材料。16
导电金属氧化物的带隙为0 eV或更小,这意味着电子可以轻松地从价带移动到导带。这允许电子自由流动,从而使材料具有导电性。17导电金属氧化物的一些例子包括ZnO、SnO 2、NiO、Cu 2 O、In 2 O 3和MnO 2。二氧化锰(MnO 2)因其理论容量大和工作电压高而被普遍认为是最有前途的候选材料之一。18二氧化锰是良好的电导体,因为它具有部分填充的 3d 电子壳层。这意味着电子可以自由移动,从而允许电流流动。19 MnO 2的电导率取决于多种因素,包括部分填充的 3d 电子壳层、晶体结构和温度。这使得MnO 2成为用于多种应用的有用材料,包括电池、20传感器、21超级电容器22和催化剂。23李等人。2012年报道称MnO 2可用作导电材料以提高储能装置的电化学性能。24
为了实现MnO 2在铅酸电池中 的实际应用,我们配制了一种包含MnO 2作为添加剂的PVA基凝胶电解质。我们使用傅里叶变换红外光谱(FTIR)技术来了解 PVA 和 MnO 2之间的相互作用。对凝胶系统进行了循环伏安法(CV)、电化学阻抗谱(EIS)、动电位极化(PDP)和恒电流充放电(GCD)测试等电化学测试,以分析其电化学行为。PVA凝胶中添加MnO 2后离子电导率的增加证明MnO 2 @PVA凝胶体系可用于增强VRLA电池的电化学性能。
实验性的
化学品
聚乙烯醇(M w ∼ 124 000)购自印度孟买的 SD Fine Chemicals Ltd。二氧化锰(M w ∼ 86.94)由印度钦奈的 Reachem Laboratory Chemicals Private Limited 提供。硫酸由 Spectrum Reagent and Chemicals Pvt. 提供。有限公司,印度科钦。整个实验过程中使用软化水。
凝胶系统的配制
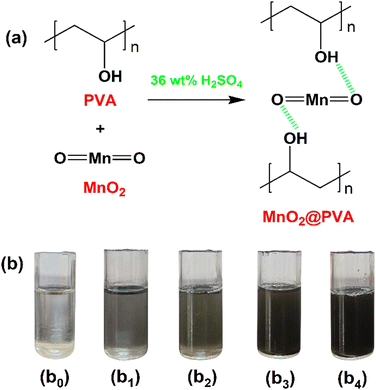
通过在60℃下加热并连续搅拌直至形成均匀的粘稠溶液, 将4wt%的PVA溶解在36wt%的H 2 SO 4中,制备PVA凝胶电解质。所得凝胶电解质称为平面PVA。为了制备掺有MnO 2的PVA凝胶电解质,将已知量的MnO 2添加到PVA凝胶电解质中并将溶液在室温下搅拌24小时。然而,关于PVA的MnO 2的量变化为1、3、5和7wt%,并且所得凝胶电解质被指定为1wt%MnO 2 @PVA、3wt%MnO 2 @ PVA、5wt%MnO 2 @PVA 和 7 wt% MnO 2分别@PVA。图1(a)表示MnO 2和PVA之间的氢键相互作用。图 1(b)显示了合成凝胶系统的照片图像。
凝胶体系的特性研究
为了确定凝胶结构中 MnO 2和 PVA 之间的相互作用,将凝胶进行 FTIR 分析(PerkinElmer Pvt. Ltd,新加坡)。使用 EQ-662 型电导率计(Equip-Tronics,印度孟买)测量凝胶的离子电导率。使用 CV、EIS、PDP 和 GCD 等技术来检查凝胶制剂的电化学性质。记录 CV 曲线时,使用10 至 100 mV s -1之间的多个扫描速率,同时保持 -1 至 +1 V 的电位范围。在每个 OCP 处,在 1 Hz 至 100 kHz 的频率范围内进行 EIS 测量幅度为 5 mV。通过了解各种 OCP,PDP 测试以 10 mV s -1的扫描速率进行。我们设计了一种采用改进的凝胶电解质的原型电池,为了评估其运行方式,在不同电流密度下进行了 GCD 测试以及循环分析。在电化学分析仪(CHI660E,CH Instruments,德克萨斯州,美国)中,我们采用了用于 CV、EIS 和 PDP 的三电极系统以及用于 GCD 的两电极系统。铅电极、铂丝和 Ag/AgCl、(饱和)KCl 分别是工作电极、对电极和参比电极。分析之前,将铅电极抛光,注意避免接触电极。所有实验均在 25 °C 温度下进行。
结果与讨论
红外光谱分析
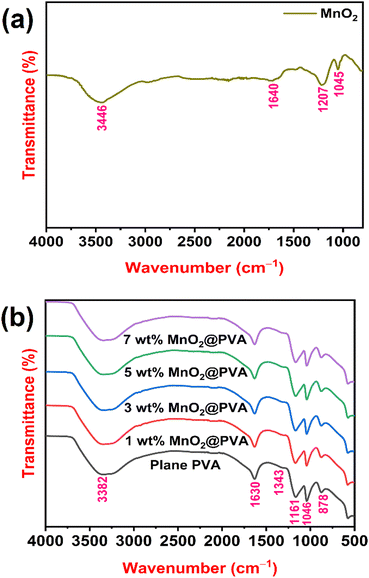
MnO 2粉末 的FTIR光谱如图2(a)所示。O-H伸缩振动归因于约3446 cm -1的宽带,表明MnO 2是水合物。25被吸收的水分子的 O-H 基团的弯曲振动可能是 1640 cm -1处弱带的原因。与Mn原子耦合的26 O-H被认为是约1207 cm -1和1045 cm -1吸收带中弯曲振动的来源。27图 2(b)显示了平面 PVA 和负载不同 wt% MnO 2的 PVA 的 FTIR 光谱。在3382、1630、1161和1046cm -1处观察到PVA的主峰。3382 cm -1处的峰归属于羟基的O-H伸缩振动。CO![[双键,长度为m-破折号]](https://www.rsc.org/images/entities/char_e001.gif) 羰基拉伸导致1630cm -1处的峰。28 1161 cm -1和 1046 cm -1处的两个峰对应于乙酰基的 C-O 伸缩。29随着 PVA 基体中 MnO 2含量的增加,这些特征峰的扩展略有减小,表明聚合物基体中MnO 2含量的影响。这也表明MnO 2颗粒插在PVA链之间,限制了聚合物链的流动性并减小了层间距。30此外,1343 cm -1和878 cm -1处的峰与凝胶体系中H 2 SO 4
羰基拉伸导致1630cm -1处的峰。28 1161 cm -1和 1046 cm -1处的两个峰对应于乙酰基的 C-O 伸缩。29随着 PVA 基体中 MnO 2含量的增加,这些特征峰的扩展略有减小,表明聚合物基体中MnO 2含量的影响。这也表明MnO 2颗粒插在PVA链之间,限制了聚合物链的流动性并减小了层间距。30此外,1343 cm -1和878 cm -1处的峰与凝胶体系中H 2 SO 4![[双键,长度为m-破折号]](https://www.rsc.org/images/entities/char_e001.gif) 中SO 和S-OH的伸缩振动有关。31,32
中SO 和S-OH的伸缩振动有关。31,32
离子电导率研究
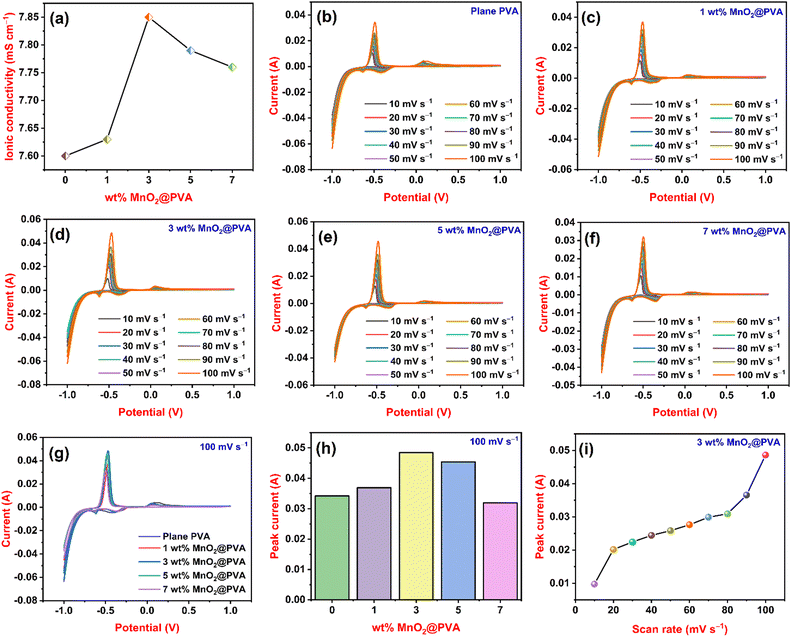
离子电导率是由于离子电荷运动而产生的电导率。33图 3(a)显示了所有凝胶系统的离子电导率结果。平面PVA或0wt%MnO 2 @PVA的离子电导率为7.6mS cm -1。MnO 2 @PVA凝胶体系的离子电导率值高于平面PVA。1 wt% MnO 2 @PVA、3 wt% MnO 2 @PVA、5 wt% MnO 2 @PVA 和 7 wt% MnO 2 @PVA 凝胶电解质的离子电导率为 7.63、7.85、7.79 和 7.76 mS cm -1,分别。MnO 2含量PVA凝胶体系中的含量从1wt%增加到3wt%,离子电导率也增加。这是因为 MnO 2颗粒与聚合物链相互作用,形成更加开放和灵活的网络。这使得离子更容易穿过电解质,从而产生更高的离子电导率。34此外,在 5 wt% MnO 2和 7 wt% MnO 2 @PVA 凝胶体系中观察到离子电导率呈下降趋势。随着溶液粘度的增加,离子移动的时间变得更加困难,从而降低了离子电导率。35
简历分析
循环伏安法是一种强大且广受欢迎的电化学方法,它经常用于研究化学物质的还原和氧化过程。36图3(b)、(c)、(d)、(e)和(f)表示平面PVA、1 wt% MnO 2 @PVA、3 wt% MnO 2 @PVA、5 wt% MnO的循环伏安图分别为2 @PVA和7wt%MnO 2 @PVA凝胶电解质。我们以 10 mV s -1至 100 mV s -1的不同扫描速率记录循环伏安图。尖锐的阳极和阴极峰代表氧化还原反应的发生。-0.47V处的阳极峰和-0.61V处的阴极峰分别代表从铅形成硫酸铅和从硫酸铅形成铅。大约0V处的阳极峰和-0.39V处的阴极峰分别表明铅电极中痕量锑的氧化以及从氧化铅形成铅。37从所有循环伏安图中可以看出,随着扫描速率的增加,峰值电流也会增加。峰值电流与电活性物质扩散到电极表面的速率成正比。38随着扫描速率的增加,可用于扩散的时间减少,因此电流必须增加才能维持相同数量的电荷转移。图3(g)显示了所有凝胶系统在100 mV s -1固定扫描速率下的循环伏安图,图3(h)显示了扫描时不同wt%MnO 2 @PVA的峰值电流的变化100 mV s -1的速率。对于平面 PVA、1 wt% MnO 2 @PVA、3 wt% MnO 2 @PVA、5 wt% MnO 2 @PVA 和 7 wt %,获得了 0.0342 A、0.0369 A、0.0485 A、0.0454 A 和 0.0319 A 的峰值电流。分别为%MnO 2 @PVA凝胶电解质。由图3(g)和(h)可知,观察到3 wt% MnO 2 @PVA 在所有凝胶体系中表现出最高的峰值电流。随着PVA中MnO 2的含量从1wt%增加到3wt%,峰值电流由于PVA凝胶基质中MnO 2活性位点的增加而增加。在PVA中进一步添加MnO 2从5wt%到7wt%导致峰值电流降低。这是由于凝胶结构变形或凝胶网络变弱所致。图3(i)显示了3 wt% MnO 2 @PVA凝胶体系在不同扫描速率下峰值电流的变化。在这种情况下,峰值电流也随着扫描速率的增加而继续增加。CV结果表明3 wt% MnO 2@PVA凝胶系统是一种优化的凝胶电解质。
电化学阻抗谱分析
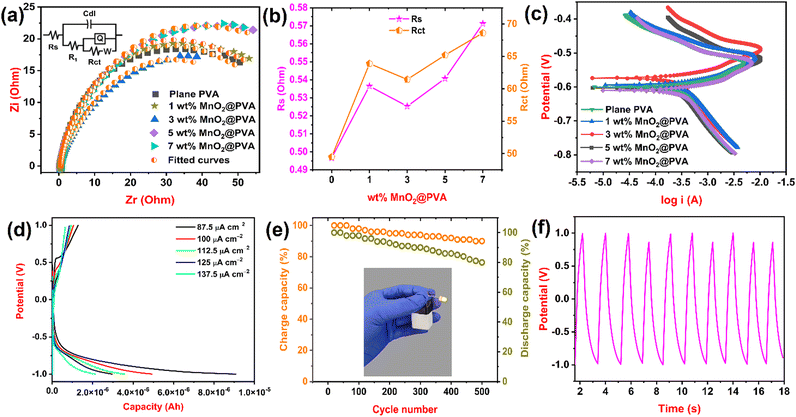
电化学阻抗谱是一种用于表征电化学系统电性能的强大技术。它是一种无损技术,可用于研究各种系统,包括电池、燃料电池、腐蚀和生物系统。39图4(a)显示了平面PVA和负载不同MnO 2的PVA的奈奎斯特图以及等效电路。我们使用ZSimpWin 3.21软件绘制拟合曲线并选择等效电路。我们使用R(电阻)、C dl(双层电容)、Q(恒相元件)和W等阻抗参数(Warburg 阻抗)测量配制的凝胶电解质的阻抗性质。R s(溶液电阻)和R ct(电荷转移电阻)是测量凝胶系统电阻行为的关键发现。表 1展示了所有配制的凝胶系统的阻抗结果。从图4(b)和表1中可以看出,3wt%MnO 2 @PVA凝胶体系具有较低的R s (0.5253 Ohm)和R ct (61.44 Ohm)值以及较高的C值dl (0.0002015 F) 和Q (0.004342 S s n) 与其他负载 MnO 2的 PVA 凝胶相比。这是由于在该浓度下存在更多可移动离子,这些离子可以携带电流,从而降低电阻,从而增加电导。40 3 wt% MnO 2 @PVA 凝胶系统还显示出较低的 Warburg 阻抗值 (0.05048 S s 5 )。这意味着离子到达电极需要更长的时间,从而导致较低的 Warburg 阻抗。EIS结果显示3 wt% MnO 2 @PVA凝胶体系是优化的凝胶电解质,这与CV结果非常吻合。
| 凝胶系统 | Rs (欧姆) | C dl (F) | R 1(欧姆) | Q (S s n ) | n | Rct (欧姆) | W (S s 5 ) | E校正(V) | 我错了(A) |
|---|---|---|---|---|---|---|---|---|---|
| 平面聚乙烯醇 | 0.4966 | 0.0001827 | 3.828 | 0.002173 | 0.63 | 49.48 | 0.06794 | −0.6058 | 3.5431 |
| 1 wt% MnO 2 @PVA | 0.5365 | 0.0002001 | 4.696 | 0.002209 | 0.58 | 63.89 | 0.08516 | −0.5901 | 3.5102 |
| 3 wt% MnO 2 @PVA | 0.5253 | 0.0002015 | 2.991 | 0.004342 | 0.62 | 61.44 | 0.05048 | −0.5894 | 3.3641 |
| 5 wt% MnO 2 @PVA | 0.5407 | 0.0001881 | 6.299 | 0.002359 | 0.63 | 65.19 | 0.05583 | −0.6037 | 3.4347 |
| 7 wt% MnO 2 @PVA | 0.5712 | 0.0001832 | 7.847 | 0.001915 | 0.61 | 68.61 | 0.05727 | −0.6116 | 3.524 |
等离子显示分析
腐蚀测试中最常用的直流电化学技术之一是动电位极化测量。由于等离子显示面板中测试电极的电位范围很大,因此主要发生金属表面氧化或还原过程,从而产生适当的电流。41图4(c)显示了平面PVA 和负载MnO 2的PVA 的动电位极化曲线。腐蚀电流 ( I corr ) 和腐蚀电位 ( E corr ) 是凝胶系统要分析的参数。配制的凝胶系统的I corr和E corr值在表 1中给出。从表中可以看出,3 wt% MnO 2 @PVA 凝胶系统具有较低的I corr (3.3641 A) 和E corr (-0.5894 V) 值。I corr值越低表示腐蚀速率越慢。这意味着离子更难穿过凝胶,从而减慢了腐蚀反应。42 PDP 结果帮助我们知道 3 wt% MnO 2 @PVA 凝胶系统是一种优化的凝胶电解质,与 CV 和 EIS 结果非常一致。
GCD分析
恒电流充放电是一种以恒定电流对器件进行电化学充电和放电的方法。由于其与电容充电的物理联系非常密切,它也被用来描述超级电容器和二次电池。43我们填充了 3 wt% MnO 2 @PVA 凝胶电解质,将其优化为原型电池,并在不同电流密度下进行了 GCD 测试。图4(d)示出了与电位有关的容量曲线。该电池在电流密度137.5、125、112.5、100和87.5 μA cm -2下的放电容量分别为2.143、2.972、3.593、4.948和9.080 μA h, 分别。当电流密度较低时,电池有更多时间进行电化学反应并释放其存储的能量。因此,随着电流密度降低,电池的放电容量增加。44该电池在87.5 μA cm -2的电流密度下显示出9.080 μA h 的最大放电容量。电池使用的循环研究是一种测量电池在损失大量容量之前可以充电和放电的次数的测试。我们对包含优化凝胶电解质的电池在140 μA cm -2的电流密度下进行了500次循环的循环研究。图4(e)显示电池的循环寿命相对于充电和放电容量的百分比。经过500次长时间循环后,电池的放电容量为81%,表现出良好的循环稳定性。45当电池放电时,电极中的活性材料会发生化学反应,释放电子。这些反应是可逆的,但随着时间的推移,它们的效率会降低,从而导致放电容量下降。46图 4(e)还显示了用于点亮 LED 的电池的照片图像。循环研究期间充放电曲线的性质如图4(f)所示。因此,我们使用 3 wt% MnO 2@电池中的 PVA 凝胶电解质并使用 GCD 技术展示了其工作原理。
结论
在这项研究工作中,我们为 VRLA 电池 配制了负载不同量 MnO 2的 PVA 基质凝胶系统。FTIR 中特征峰的扩展略有下降表明PVA 凝胶基质中MnO 2的影响。从离子电导率研究中可以看出,3 wt% MnO 2 @PVA 凝胶电解质的最大离子电导率为 7.85 mS cm -1。在CV 分析中,对于3 wt% MnO 2 @PVA 凝胶电解质观察到最高阳极峰值电流为0.0369 A。EIS 技术表明,3 wt% MnO 2 @PVA 凝胶电解质是优化的凝胶系统,因为它具有较低的R s (0.5253 Ohm) 和RCT(61.44 欧姆)值。PDP技术的结果表明,3 wt% MnO 2 @PVA凝胶电解质具有最低的I corr值,为3.364 A。此外,包含3 wt% MnO 2 @PVA凝胶电解质的原型电池的GCD技术表现出最高的放电率在87.5 μA cm -2的电流密度下,容量为9.080 μA h 。500次循环后,电池显示出81%的放电容量。所有这些电化学发现表明MnO 2可以提高VRLA电池的性能。
- 上一篇:JLG电池化学与技术
- 下一篇:垂直起降机载电动汽车电池
